Pomůcky
Voltmetr Vernier DVP-BTA nebo Vernier VP-BTA, rozhraní LabQuest Mini, citron, nůž, mince 5 Kč a 10 Kč, hliníková vidlička.
Teorie
V galvanických článcích vzniká elektrické napětí mezi dvěma různými kovy (elektrodami) umístěnými v elektrolytu. V níže popsaném provedení experimentu je elektrolyt představován citronovou šťávou (zředěná kyselina citronová) a jako elektrody jsou používány běžně dostupné předměty - desetikoruna (měděný povrch), pětikoruna (niklový povrch) a hliníková vidlička.
Příprava měření
- Pomocí USB kabelu připojte rozhraní LabQuest Mini k počítači.
- Do rozhraní LabQuest Mini zapojte voltmetr DVP-BTA nebo voltmetr VP-BTA.
- Na počítači spusťte program Logger Lite.
- Vynulujte aktuálně měřenou hodnotu napětí (menu Experiment → Nulovat).
- Pomocí myši klikněte na okno s číselným údajem (vlevo dole) a tažením za roh okna roztáhněte toto okno na celou obrazovku tak, jak ukazuje obrázek níže.
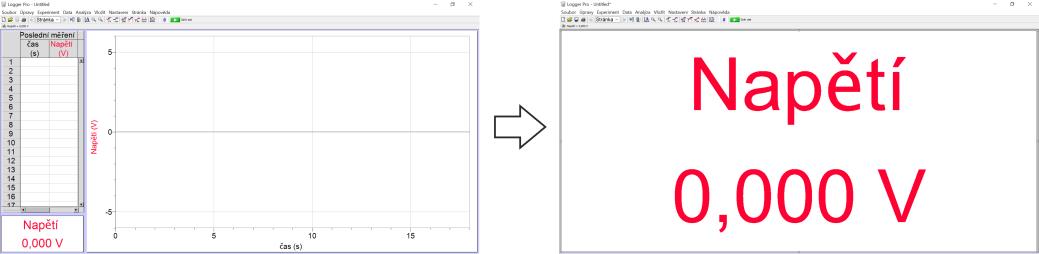
Provedení experimentu
- Nožem rozkrojte citron na dvě poloviny, potřebovat budete jednu z nich.
- Do poloviny citronu natlačte větší část desetikorunové mince a část hliníkové vidličky. V místě vkládání mince je výhodné citron předem proříznout.
- Na oba kovové předměty připojte vodiče voltmetru (obrázek na protější straně) a poznamenejte si měřenou hodnotu napětí.
- Body 2 a 3 zopakujte také pro dvojice pětikoruna-vidlička a pětikoruna-desetikoruna.

Ukázka naměřených dat
Pro tři uvedené dvojice předmětů (kovů) byly získány následující hodnoty napětí:
|
dvojice předmětů
|
příslušné kovy
|
napětí
|
|
desetikoruna - vidlička
|
měď - hliník
|
0,6 V
|
|
pětikoruna - vidlička
|
nikl - hliník
|
0,5 V
|
|
pětikoruna - desetikoruna
|
nikl - měď
|
0,2 V
|
Závěr
Různé dvojice kovů generují při vložení do téhož elektrolytu (citronové šťávy) různá napětí. V našem měření poskytuje nejvyšší napětí dvojice měď - hliník, nejnižší pak dvojice nikl - měď.
Poznámky
- Je třeba dát pozor, aby se kovy vně ani uvnitř citronu nedotýkaly. Stejně tak je třeba dbát, aby se elektrolyt nedostal ke svorkám voltmetru.
- Naměřené hodnoty se v tomto experimentu vždy budou lišit od standardních potenciálů uváděných u Beketovovy řady kovů. Příčinou je to, že podmínky experimentu se liší od standardizovaných.
- Zkuste místo citronu použít i jiné elektrolyty, např. slanou vodu.
- Zkuste provést experiment i sjinými kovy.
Tento experiment vychází z tzv. Kuchařky (souboru jednoduchých experimentů do hodin chemie, fyziky a přirodopisu), která vznikla na KDF MFF UK jako společné dílo Pavla Böhma, Jakuba Jermáře a Petra Kácovského.


